Tabla de contenidos
Introducción
Las moléculas que más abundan en las células son las proteínas, si exceptuamos al agua. Las proteínas son grandes moléculas fundamentales por la importancia de sus funciones. Entre estas funciones se encuentran la catálisis de reacciones químicas, transportan sustancias, participan en la defensa de los organismos…. Aún con su gran importancia, tienen estructuras relativamente simples. Todas las proteínas están formadas por otras más sencillas, los aminoácidos. Los aminoácidos se unen para formar proteínas, es decir, son los monómeros de las proteínas.
Definición
Un aminoácido es una molécula, donde a un átomo de carbono se le unen cuatro grupos químicos distintos:
- un grupo amino (-NH2)
- un grupo ácido (-COOH)
- otro grupo que es distinto en cada aminoácido. Este grupo hace a los aminoácidos diferentes entre sí, el radical «R»
- un átomo de hidrógeno (H)
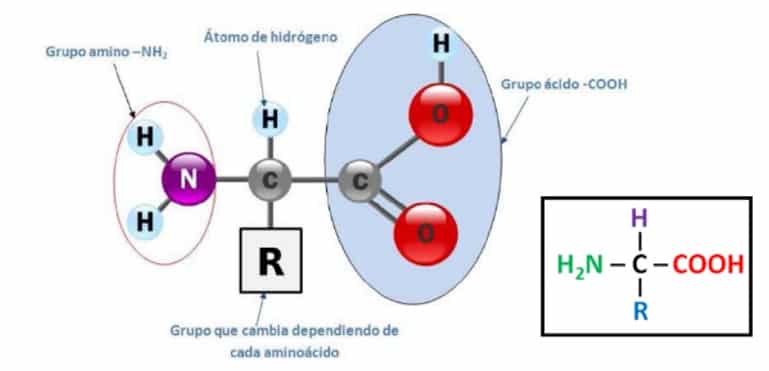
Los cuatro grupos que rodean al carbono ayudan a que una proteína logre la estructura que determina la función de la proteína.
Según la cantidad de aminoácidos que se unan, así tenemos: un dipéptido si se unen dos; un tripéptido si se unen tres….y en general, hasta quince unidos se les llama oligopéptidos. Hasta cincuenta unidos se les denomina polipéptidos. Y ya, si se unen más, a esas cadenas que se forman, se les llama proteínas, que pueden contener incluso más de mil.
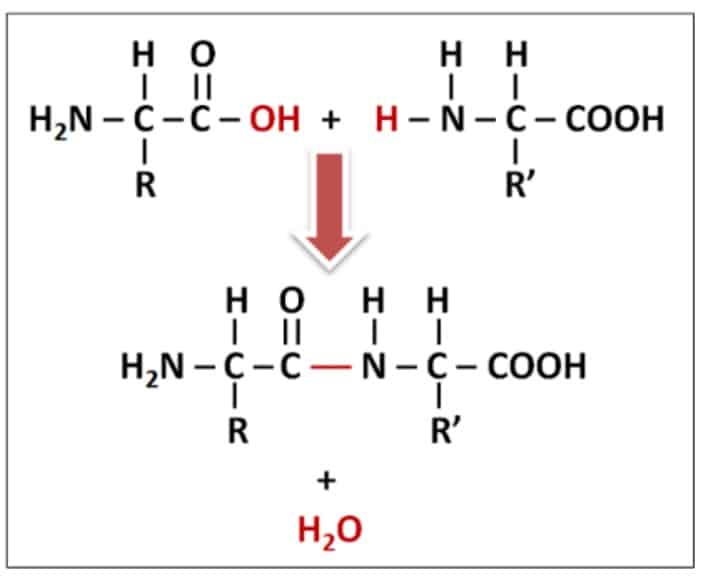
El enlace por el que se unen los aminoácidos para formar las proteínas es el enlace peptídico. Se trata de un enlace covalente entre el grupo amino de un aminoácido y el grupo carboxilo del otro. En la reacción de formación del enlace peptídico se desprende una molécula de agua. El enlace peptídico no permite giros, y es determinante para la configuración espacial de las proteínas.
Son unos quinientos los aminoácidos que se han identificado en la naturaleza. Pero son solo una veintena de ellos los que forman las proteínas en el ser humano. Estos pueden clasificarse según sea capaz el cuerpo de no producirlos o producirlos, en “esenciales” y “no esenciales”. Esta clasificación puede variar dependiendo según la especie. Además hay discrepancia entre algunos autores a la hora de clasificarlos.
Aminoácidos esenciales y no esenciales
Los aminoácidos esenciales son aquellos que no pueden ser producidos por el cuerpo humano. En consecuencia, los debemos obtener a través de la alimentación. Son nueve: lisina, valina, leucina, isoleucina, metionina, fenilalanina, treonina, triptófano e histidina.
Los aminoácidos no esenciales son aquellos que podemos obtenerlos de alimentos, pero que además nuestros cuerpos pueden sintetizarlos. Estos son arginina, alanina, ácido aspártico, asparagina, cisteína, ácido glutámico, glutamina, glicina, serina, prolina y tirosina.
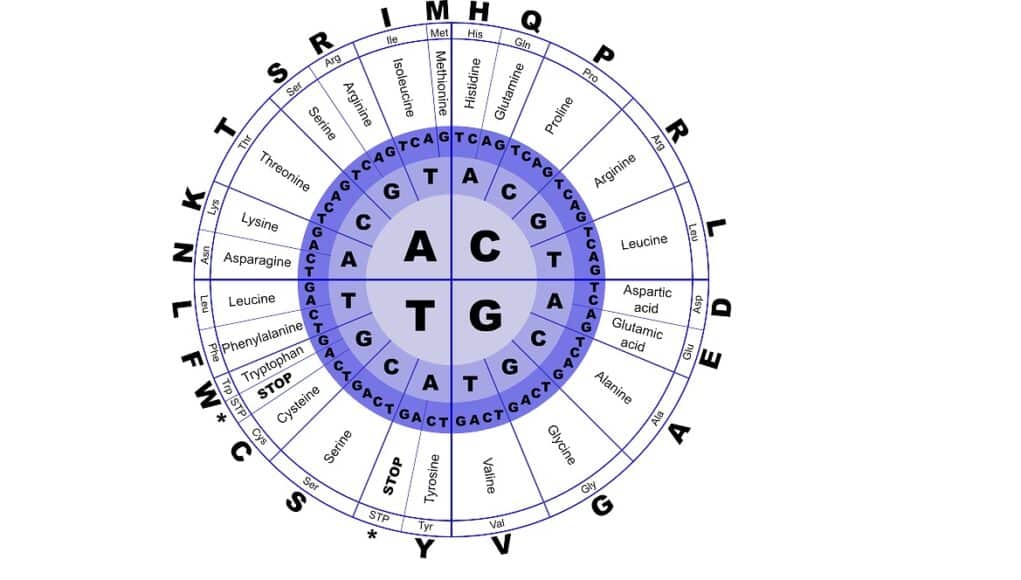
Las proteínas son muy diversas. Para la mayoría de los seres vivos, son los veinte aminoácidos anteriores los que se combinan para formar las proteínas. Dependiendo de la cantidad, del tipo de aminoácido y del orden en el que estén colocados, así será una proteína u otra la que se forme. En la siguiente figura tienes estos veinte aminoácidos:
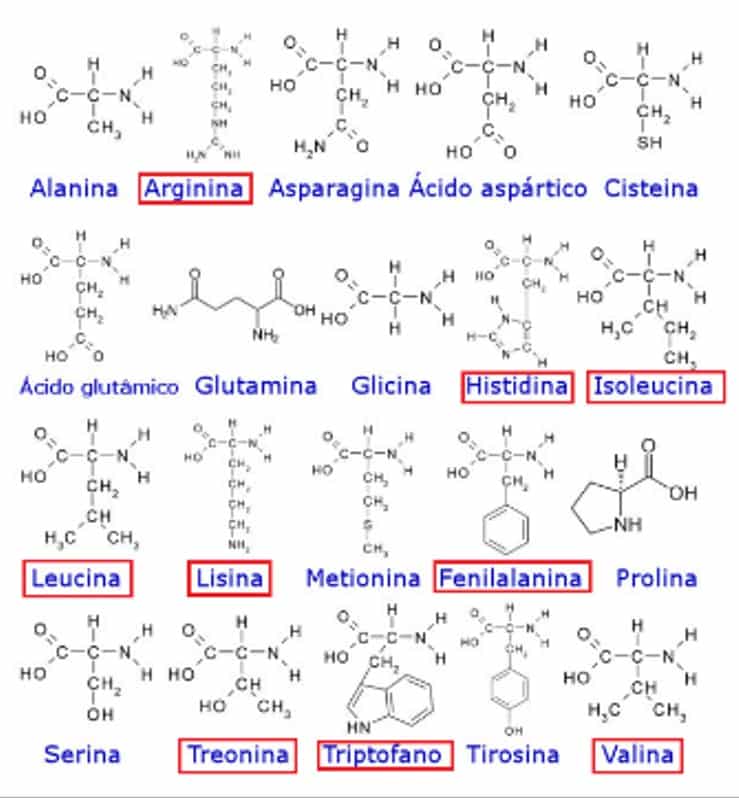
Los que están recuadrados en rojo son aquellos que deben ser captados a través de los alimentos y no pueden ser sintetizados por el ser humano, los esenciales.
Clasificación de los aminoácidos proteicos según los grupos R
Los aminoácidos pueden también clasificarse según su radical R, en:
- Neutros no polares (hidrófobos). Tienen igual número de radicales amino que carboxilo. No tienen grupos R que puedan formar enlaces por puentes de hidrógeno. Por ello, no solubles en agua.
- Neutros polares sin carga. Tienen R que pueden formar enlaces por puentes de hidrógeno. Son más solubles en agua que los no polares.
- Ácidos. Tienen mayor número de radicales carboxilo que amino, y su carga neta es negativa.
- Básicos. Con mayor número de radicales amino que carboxilo, y su carga neta es positiva.
Propiedades de los aminoácidos
Para finalizar, aquí os dejo un resumen de las propiedades físico-químicas de los aminoácidos.
- Se comportan como ácidos a un pH básico, como bases a un pH ácido.
- Son determinantes en la forma de las proteínas.
- Son moléculas polares, solubles en agua y cristalizan.
- Tienen alto punto de fusión.
- Presentan isomería espacial, al igual que los monosacáridos. Esto es debido a que tienen carbonos asimétricos.
- Tienen actividad óptica, pues presentan isomería óptica.
Más contenidos en www.loreseek.com
Síguenos en Twitter: @LoreSeekWeb y en Facebook: LoreSeekWeb
Estamos en Instagram: @loreseek